O câncer é uma doença assustadora e, à primeira vista, parece mais mortal do que nunca. Ele vitima cerca de 10 milhões de pessoas por ano, um número que vem crescendo de forma constante nas últimas décadas.
Em países ricos, metade dos homens e um terço das mulheres desenvolvem a doença em algum momento da vida. Em muitos lugares, como Austrália, Reino Unido, Canadá e Japão, as pessoas têm mais chances de morrer de câncer do que por qualquer outra causa.
Esses números alarmantes, porém, são em grande parte fruto da demografia. À medida que a população mundial cresce, o número de mortes por câncer também aumenta. O envelhecimento populacional tem o mesmo efeito, já que o câncer pode levar décadas para se desenvolver e, por isso, afeta com mais frequência os idosos do que os jovens.
Se você excluir os efeitos do crescimento populacional e do envelhecimento, a taxa de mortalidade por câncer, na verdade, caiu significativamente nos últimos 30 anos. Ele está se tornando muito menos letal — e os rápidos progressos no entendimento da doença por parte dos cientistas indicam que mais avanços estão a caminho.
A queda na taxa de mortalidade é fruto de uma série de avanços em prevenção, diagnóstico e tratamento. O maior impacto vem da redução no tabagismo — responsável por cerca de 85% dos casos de câncer de pulmão e por 20% de todas as mortes por câncer no mundo.
Exames como mamografia, colonoscopia e papanicolau, entre outras formas de rastreamento, ajudam a identificar lesões, pólipos e outras alterações com potencial de se tornarem cancerígenos, mas que podem ser removidos antes disso, interrompendo a progressão.
Técnicas cirúrgicas e melhores medicamentos também aumentam as chances de sobrevivência para quem desenvolve a doença. Nos últimos anos, a imunoterapia — que estimula o sistema imunológico do próprio paciente a combater o câncer com mais eficiência — teve um avanço surpreendente.
Estima-se que esses avanços tenham evitado 6 milhões de mortes nos Estados Unidos entre 1975 e 2020. Essa estimativa considera apenas os casos de câncer de pulmão, mama, intestino, próstata e colo do útero — que, juntos, representaram cerca de 70% das mortes por câncer no fim dos anos 1970.
Pouco mais da metade das mortes evitadas deveu-se à redução no tabagismo. Outros 23% foram atribuídos à melhora no rastreamento precoce e 20%, aos avanços nos tratamentos.
O câncer de estômago, que antes era comum em países ricos, também caiu drasticamente. Nos anos 1990, pesquisadores identificaram que ele era frequentemente causado pela bactéria Helicobacter pylori. As infecções por ela já estavam em queda desde os anos 1950, devido à melhoria das condições de higiene e ao uso mais amplo de antibióticos, mas essa descoberta levou ao desenvolvimento de testes e tratamentos específicos, reduzindo ainda mais a incidência desse tumor.
Um problema a menos
Talvez o avanço mais marcante diga respeito à prevenção do câncer do colo do útero. No início do século XX, ele era o câncer mais letal entre as mulheres nos EUA.
O primeiro avanço veio com a constatação de que certas alterações nas células do colo do útero, visíveis ao microscópio, frequentemente evoluem para câncer. Isso levou à criação de programas de rastreamento para detectar e remover tecidos suspeitos antes que se tornassem malignos.
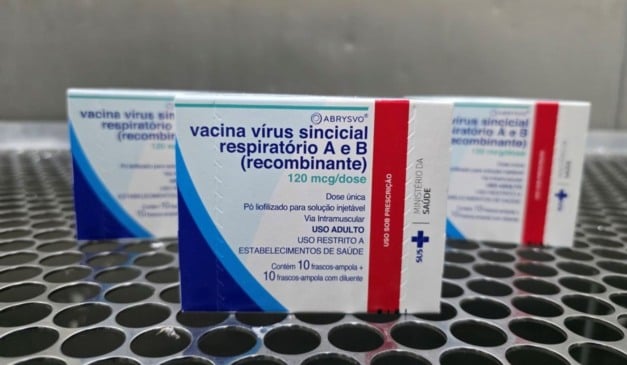
A análise das muitas amostras coletadas nesses exames levou à descoberta de que quase todos os casos de câncer do colo do útero são causados por infecção pelo papilomavírus humano (HPV). O desenvolvimento de vacinas contra o vírus abriu caminho para a quase erradicação desse tipo de câncer.
No Reino Unido, a vacinação levou a uma queda de 90% nos casos de câncer do colo do útero entre mulheres na faixa dos 20 anos — considerando dados do primeiro grupo a quem o imunizante foi oferecido aos 12 ou 13 anos de idade.
O sucesso no combate aos tumores no pulmão e colo do útero tornou-se um modelo para que os cientistas buscassem maneiras de prevenir outros tipos de câncer.
Eles aprenderam que o primeiro passo é identificar quem está em maior risco de desenvolver a doença e, em seguida, intervir da forma mais eficaz — convencer fumantes a parar de fumar e vacinar jovens contra o HPV, por exemplo.
É verdade que a maioria dos cânceres é mais difícil de enfrentar, pois suas causas são mais complexas e menos compreendidas. Apenas cerca de metade dos casos pode ser explicada por fatores de risco conhecidos.
A grande quantidade de amostras de tecido coletadas ao longo dos anos, juntamente com os avanços na biologia celular, contudo, tem tornado mais fácil identificar padrões e personalizar tratamentos.
Várias novas vacinas desenvolvidas a partir dessas pesquisas já estão em andamento. Esses dados também ajudam na identificação de medicamentos profiláticos. A esperança é que, em vez de tratar o câncer somente após seu desenvolvimento, muitos tipos da doença possam ser prevenidos.
Um longo caminho
“O câncer não surge do nada”, diz Sarah Blagden, da Universidade de Oxford. Ele se desenvolve lentamente ao longo de muitos anos, o que oferece amplas oportunidades para intervenção médica.
O processo começa quando mutações genéticas fazem com que células normais se reproduzam de maneira anormal. À medida que se dividem, algumas dessas células defeituosas adquirem características que as ajudam a escapar do sistema imunológico, que normalmente elimina células danificadas ou doentes. Com o tempo, elas formam aglomerados de tecido chamados de lesões, pólipos ou tumores.
Essas lesões podem levar de 5 a 15 anos para se desenvolver. Quando atingem tamanho suficiente, podem ser detectadas por mamografias, colonoscopias e outros exames semelhantes. Algumas param de crescer ou até regridem, mas outras evoluem para um câncer plenamente desenvolvido. Assim, passam a invadir camadas de tecido além daquelas onde surgiram inicialmente e, eventualmente, se espalham pelo corpo (um processo chamado metástase, que pode levar de 5 a 10 anos a mais).
A maioria dos programas de rastreamento de câncer tem como objetivo detectar lesões e removê-las antes que se tornem malignas. Mas ainda é difícil saber quem deve ser submetido a exames regulares e quais lesões, uma vez identificadas, realmente precisam ser retiradas.
O rastreamento costuma ser baseado em critérios muito amplos — como idade ou histórico de câncer na família. Com isso, muitas pessoas que não apresentam risco elevado acabam sendo submetidas a exames desnecessários, inclusive procedimentos invasivos que podem causar danos. Colonoscopias, por exemplo, podem perfurar o intestino; biópsias da mama, do pulmão ou de outros tecidos podem causar infecções e outras complicações.
Além disso, apenas cerca de 25% do tipo mais comum de lesão encontrada no tecido mamário evolui para câncer. Da mesma forma, embora a maioria dos cânceres colorretais se origine a partir de pólipos, apenas entre 5% e 10% dos pólipos realmente se tornam câncer.
Cientistas da University College London descobriram que, se não forem tratadas, 30% das lesões pulmonares de um tipo específico regridem espontaneamente com o tempo. Mesmo assim, todas essas lesões são tratadas como se fossem câncer em estágio inicial, já que ainda não há como prever com segurança quais delas vão se tornar malignas. O resultado é um grande número de cirurgias, radioterapias e quimioterapias desnecessárias — tratamentos caros e desgastantes.
Uma possível solução para o “lado B” desses exames de rastreio seria o desenvolvimento de métodos de triagem mais baratos e menos invasivos para detectar lesões — e, de fato, muitos estão em desenvolvimento, incluindo testes de ar expirado, sangue e urina.
Melhor ainda seria identificar com mais precisão quem realmente está em risco, para direcionar o tratamento apenas a quem precisa. Os cientistas também têm avançado nessa frente, de duas maneiras: identificando predisposições genéticas e estudando quais proteínas no sangue ou nos tecidos podem servir como “biomarcadores” de maior risco de desenvolver câncer.
Cerca de 5% a 10% dos casos de câncer parecem ter origem genética. Aproximadamente 1 em cada 200 pessoas possui mutações nos genes BRCA1 e BRCA2, que estão envolvidos na supressão de tumores, por exemplo. Em mulheres, essas alterações genéticas conferem um risco de 60% a 80% de desenvolver câncer de mama ou de ovário.
Uma em cada 300 pessoas apresenta a síndrome de Lynch, causada por mutações em genes relacionados à reparação do DNA. Essas pessoas têm de 40% a 80% de chance de desenvolver câncer colorretal, de endométrio, entre outros.
Embora sejam casos extremos, muitos outros genes também parecem aumentar o risco de certos cânceres. Como os genes são herdados, é fácil identificar quem deve ser testado para essas mutações e, a partir daí, monitorar essas pessoas mais de perto em busca de sinais da doença.
Estilo de vida
Outro conjunto de pistas sobre quem está em risco vem de grandes estudos médicos conduzidos nas últimas décadas para examinar a relação entre dieta, estilo de vida e câncer.
Alguns deles, como o projeto EPIC — que acompanha 500 mil europeus há quase 30 anos —, criaram “biobancos” de amostras de sangue. Isso permite que os pesquisadores analisem o sangue de participantes que desenvolveram câncer, bem como compará-lo com o de quem não desenvolveu, para tentar encontrar características distintivas.
Em especial, eles vêm investigando proteínas que são mais comuns em pacientes que desenvolvem câncer. Essas pesquisas mostraram que pessoas com níveis elevados de uma proteína que estimula o crescimento celular — o fator de crescimento semelhante à insulina (IGF) — têm maior risco de desenvolver câncer de mama e de intestino.
As amostras de biobancos também ajudaram uma equipe liderada por Marc Gunter, do Imperial College London, a identificar novas proteínas que parecem ser marcadores de um risco elevado de câncer de mama. “De certa forma, elas surgiram completamente do nada”, conta ele.
Calculando o risco
Essas descobertas, além de serem individualmente relevantes, podem ser integradas a outros dados para produzir estimativas de risco mais refinadas.
Testes genéticos, exames de sangue, informações sobre dieta, atividade física e outros fatores podem ser reunidos em calculadoras de risco de câncer “multimodais”, que chegaram aos consultórios nos últimos cinco anos. Médicos utilizam-nas, por exemplo, para decidir quem deve começar a fazer exames preventivos de câncer de mama mais cedo ou tomar medicamentos preventivamente.

Rápidos avanços tecnológicos têm ajudado a aprimorar esses modelos de risco. Hoje, já é possível utilizar uma única amostra de sangue para analisar a presença de milhares de proteínas — há uma década, só seria possível investigar duas ou três.
Pesquisadores investigam se a inteligência artificial pode melhorar a predição de risco ao identificar padrões sutis em mamografias ou exames de corpo inteiro.
O desenvolvimento da transcriptômica de célula única, uma tecnologia que analisa a expressão gênica em nível celular, tornou possível observar como as células de uma amostra de tecido interagem entre si. Antes, a extração de DNA exigia triturar o tecido, o que levava à perda de informações sobre as células individualmente.
Essa e outras novas técnicas de análise têm gerado informações detalhadas sobre o funcionamento das células imunológicas, por exemplo, e sobre como detectar proteínas indicativas de câncer — o tipo de dado necessário para o desenvolvimento de medicamentos e vacinas preventivas.
Um grupo de pesquisa liderado por Walid Khaled, da Universidade de Cambridge, descobriu, por exemplo, que as células imunológicas presentes nas mamas de mulheres saudáveis com mutações nos genes BRCA são tão ineficazes quanto as encontradas em mulheres com câncer de mama avançado. O próximo passo, diz Khaled, seria identificar terapias capazes de ativar essas células.
Mais do que uma cura
Os imunizantes são outra área que avançou “tremendamente rápido” na última década, afirma Nora Disis, do Instituto de Vacinas contra o Câncer da Universidade de Washington. “Hoje temos uma noção muito melhor do tipo de resposta imunológica necessária para erradicar o câncer”, diz.
Há cinco anos, conta ela, o instituto estava focado quase exclusivamente em vacinas usadas como tratamento para casos avançados da doença. Agora, cerca de metade das pesquisas é voltada para vacinas preventivas.
Diversos grupos de pesquisa e empresas de biotecnologia nos Estados Unidos e na Europa estão testando vacinas preventivas contra o câncer de mama, de cólon e outros tipos de tumor maligno em pessoas com alto risco da doença — como aquelas com mutações nos genes BRCA, síndrome de Lynch ou lesões pré-cancerosas.
Esses imunizantes ainda estão em fases iniciais de testes. Os primeiros resultados — que devem mostrar se reduzem a recorrência de pólipos ou outras lesões — são esperados para daqui a três ou cinco anos.
Antes, diz Olivera Finn, da Universidade de Pittsburgh, havia receio de que vacinas aplicadas antes do desenvolvimento do câncer pudessem estimular o sistema imunológico a atacar células saudáveis. Mas a experiência com pacientes em estágios avançados da doença — para os quais os possíveis benefícios superavam esse risco — mostrou que o temor era infundado: o sistema imunológico, ao que parece, é bastante eficaz em direcionar sua ação apenas contra as células cancerígenas.
Ao contrário das vacinas terapêuticas contra o câncer, que muitas vezes são personalizadas de acordo com as mutações do tumor de cada paciente, as vacinas preventivas devem funcionar para uma ampla gama de pessoas.
Em um dos maiores estudos clínicos sobre a evolução de tumores pulmonares, cientistas da University College London descobriram que as células pulmonares de fumantes desenvolvem alterações específicas associadas ao câncer anos antes de a doença surgir. Pesquisadores de Oxford desenvolveram uma vacina que tem essas alterações como alvo — os testes clínicos devem começar no ano que vem.
Outra vacina preventiva, criada pela Nouscom, uma empresa suíça de biotecnologia, adota o que seus desenvolvedores chamam de abordagem “força bruta”: a injeção tem como alvo 209 fragmentos diferentes de moléculas presentes em tecidos pré-cancerosos ou cancerosos, mas ausentes em tecidos saudáveis. A primeira rodada de testes, divulgada em abril, mostrou que ela é capaz de estimular o sistema imunológico a atacar células cancerígenas — ao menos em experimentos realizados em placas de Petri.
Também está em testes clínicos uma vacina para a prevenção do câncer colorretal. Em 2023, a equipe de pesquisa de Olivera Finn divulgou resultados preliminares de uma vacina que tem como alvo uma proteína chamada MUC1, presente em 80% de todos os tipos de câncer.
Embora a vacina tenha provocado resposta imunológica apenas em uma subcategoria de pessoas com pólipos no cólon, esse grupo apresentou uma redução de 38% na reincidência deles em um período de um ano.
Medicamentos
A riqueza de dados provenientes de grandes estudos clínicos também está acelerando a identificação de medicamentos que podem ajudar a prevenir formas específicas de câncer em determinadas populações.
Pesquisadores notaram, por exemplo, que pessoas que tomam aspirina para prevenir infartos ou metformina para tratar diabetes apresentam taxas reduzidas de câncer.
Ensaios clínicos demonstraram que o anastrozol, um medicamento usado no tratamento do câncer de mama, reduz pela metade o risco de desenvolvimento da doença em algumas mulheres pós-menopausa — o que levou o órgão regulador britânico a aprová-lo, em 2023, para uso profilático.
Há estudos em andamento avaliando se esses medicamentos podem ser administrados com menos efeitos colaterais, como por meio de doses intermitentes, aplicação tópica ou injeção diretamente no tecido de interesse.
Há esperança de que agonistas do receptor de GLP-1, como o Ozempic — medicamentos promissores com diversos benefícios além do controle do diabetes — possam também ajudar a prevenir certos tipos de câncer.
Algumas dessas terapias beneficiam grupos bastante restritos de pacientes. Em 2023, pesquisadores descobriram que o uso de metformina em mulheres que tiveram um tipo específico de câncer de mama — responsável por cerca de 20% de todos os casos — reduziu a recorrência da doença. Por outro lado, o benefício do medicamento não foi visto em pacientes que tiveram outros subtipos do tumor.
Resultados como esse, que demonstram benefícios para subgrupos específicos de pacientes, estão começando a ser vistos como norma na busca por terapias preventivas contra o câncer, afirma Andrew Chan, de Harvard: “Dificilmente teremos algo como um tratamento único para todos os pacientes.”
Complexo, mas tratável
A complexidade do câncer — com sua desconcertante variedade de formas — torna difícil o desenvolvimento de tratamentos. Criar vacinas ou testar medicamentos preventivos para uma doença que pode levar 15 anos para se manifestar é, por definição, uma tarefa demorada.
Esses obstáculos ajudam a explicar por que o progresso contra a doença costuma ocorrer de forma gradual, e não por meio de avanços espetaculares. Os benefícios abrangentes das grandes medidas de saúde pública — como a redução do tabagismo ou a melhoria da higiene alimentar — já foram colhidos, ao menos nos países ricos.
Desenvolver tratamentos preventivos, combinando subgrupos específicos de pacientes com uma leque mutável de terapias, inevitavelmente exigirá um esforço de tentativa e erro. Mas os cientistas estão avançando, ainda que gradualmente, na identificação dos grupos com maior risco e na personalização dos tratamentos.
Como esse processo é contínuo e sem um ponto final definido, ele continuará gerando benefícios pelas próximas décadas. O câncer já se tornou uma doença muito menos letal do que era há 30 anos. E, dentro de 30 anos, será quase certamente menos letal do que é hoje.
*Reportagem do jornal The Economist